1. daļa
1. uzdevums.
Vai apgalvojums ir pareizs? Apvelciet atbildi ar aplīti!
| 1. |
Radioaktīvos izotopus izmanto medicīnā. |
Jā |
Nē |
| 2. |
Cukura ražošanā izmanto kaļķu pienu. |
Jā |
Nē |
| 3. |
No ogām un augļiem radušos traipus var iztīrīt ar ūdeņraža peroksīdu. |
Jā |
Nē |
| 4. |
Skābeklis saistās ar hemoglobīnu daudz ātrāk nekā oglekļa(II) oksīds. |
Jā |
Nē |
| 5. |
Latvijā ražo stikla šķiedru. |
Jā |
Nē |
| 6. |
Ožamais spirts ir amonjaka šķīdums ūdenī. |
Jā |
Nē |
| 7. |
Nemetālu oksīdi ir bāziskie oksīdi. |
Jā |
Nē |
| 8. |
Kurināmā degšana ir eksotermisks process. |
Jā |
Nē |
| 9. |
Etanāls ir etanola homologs. |
Jā |
Nē |
| 10. |
Anilīnu izmanto krāsvielu un ārstniecības līdzekļu ražošanā. |
Jā |
Nē |
2. uzdevums.
Katram jautājumam ir tikai viena pareiza atbilde. Izvēlieties pareizo atbildi un apvelciet tās burtu ar aplīti! Nepieciešamajām papildu darbībām izmantojiet lapas brīvās vietas!
1. Kura viela izdalās pie katoda, eleklrolizejot vara(II) sulfāta šķīdumu?
|
A Cu |
B S |
C H2 |
D O2 |
2. Nātrija molibdāta formula ir Na2MoO4, bet svina arsenāta formula - Pb3(AsO4)2. Svina molibdāta formula ir:
|
A PbMoO4 |
B Pb3(MoO4)2 |
C Pb2(MoO4)3 |
D Pb3(MoO4)4 |
3. Kuram savienojumam ir amfotēras īpašības?

4. Lai noskaidrotu dažādu faktoru ietekmi uz dzelzs korozijas ātrumu, dzelzs naglas ievietoja mēģenēs, kurās tika radīta dažāda vide. Kurā gadījumā dzelzs korozija norisinās visstraujāk?

5. Kurš no reakciju vienādojumiem attēlo dabas procesu, kurā palielinās ūdens cietība?
A CaCO3 +H2O + CO2 <==> Ca2++2HCO3-
B CaO+H2O <==> Ca2+ + 2OH-
C CaCO3 + 2CH3COOH - -> 2CH3COO- + Ca2+ + CO2 ^ + H2O
D Ca + 2H2O --> Ca2+ + 2OH- +H2 ^
6. Kurš grafiks attēlo ķīmiskās reakcijas ātruma (v) atkarību no temperatūras (t)?

7. Cik liels ir 0,001 M HNO3 šķīduma pH?
|
A 1 |
B 3 |
C 7 |
D 11 |
8. Reakcijā CaCO3 � MgCO3(c) <==> CaO(c) + MgO(c) +2CO2(g) - Q ķīmiskais līdzsvars ir nobīdīts reakcijas produktu rašanās virzienā, ja
|
A pazemina temperaturu, |
C izmanto katalizatoru, |
|
B palielina spiedienu, |
D samazina spiedienu. |
9. Kurā no vielām dzelzs masas daļa ir vislielākā?
|
A Fe3O4 |
B FeCO3 |
C Fe2O3 |
D FeS2 |
10. Kurš kurināmais sadegot vismazāk piesārņo vidi?
|
A Kūdra |
B Dabasgāze |
C Akmeņogles |
D Nafta |
11. Kura elementa atoma kodola lādiņš ir +7?
|
A Li |
B N |
C F |
D Fr |
12. Kurš no elementiem atrodas ķīmisko elementu periodiskās tabulas 4. periodā un VA grupā?
|
A Sn |
B As |
C Nb |
D Zr |
13. Kurā no attēliem redzama kovalentās saites veidošanās, pārklājoties s un p elektronu orbitālēm?

14. Kurš no elementiem reakcijā Ag +2HNO3 --> AgNO3 + NO2 + H2O ir oksidētājs?
|
A Ag |
B N |
C O |
D H |
15. Kura no vielām ir butanāla izomērs?

3. uzdevums.
Pabeidziet teikumus, brīvajā vietā ierakstot pareizās atbildes burtu!
1. No atomiem, molekulām vai joniem sastāv_______.
2. Oksidēšanās-reducēšanās process, kas norisinās pie elektrodiem, ja caur elektrolita šķīdumu vai kausējumu plūst līdzstrāva, ir________.
3. Atomi, kam ir vienāds kodola lādiņš, bet dažāds neitronu skaits atoma kodolā, ir_______.
4. Sāls jonu iedarbība ar ūdeni, kuras rezultātā mainās H+ un OH- jonu koncentrācija
š'ķīdumā, ir______.
5. Elektrolīti, kas ūdensšķīdumos vai kausējumos disociē, kā vienīgos anjonus veidojot hidroksīdjonus, ir______.
6. Glicerīna un augstāko karbonskābju esteri ir_______.
7. Savienojumi ar vienādu sastāvu, bet atšķirīgu uzbūvi un īpašībām ir_______.
8. Savienojumi, kuru molekulās ir karboksilgrupa un aminogrupa, ir_______.
9. Ogļhidrāts, ko satur graudi un kartupeļi,
ir_______.
10. Organismā katalītisko, regulējošo un citas funkcijas veic_______.
|
A Elektrolīze |
G Izomēri |
|
B Hidrolīze |
H Vielas |
|
C Tauki |
I Aminoskābes |
|
D Olbaltumvielas |
J Sārmi |
|
E Izotopi |
K Skābes |
|
F Ciete |
L Saharoze |
2. daļa
1. uzdevums. (8punkti)
Uzrakstiet 8 reakciju vienādojumus iespējamajām ķīmiskajām reakcijām starp dotajām vielām!
|
Vielas |
Zn |
CuO |
C2H4 |
C2H5OH |
C6H6 |
|
O2 |
1. |
2. |
3. |
4. |
5. |
|
H2 |
6. |
7. |
8. |
9. |
10. |
|
NaOH |
11. |
12. |
13. |
14. |
15. |
|
CH3COOH |
16. |
17. |
18. |
19. |
20. |
2. uzdevums. (10 punkti)
Uzrakstiet reakciju vienādojumus pārvērtībām! Ar zvaigznīti (*) atzīmētajām pārvērtībām norādiet reakciju norises apstākļus!
Slāpeklis 1*> amonjaks 2*> slāpekļa(II) oksīds 3.> slāpekļa(IV) oksīds 4.> slāpekļskābe 5.> svina(II) nitrāts 6*.> ? 7.> svins
3. uzdevums. (5 punkti)
Nātrija hidroksīda šķīduma masa ir 250,0 g, bet izšķīdinātās vielas masas daļa tajā -8,0%.
Cik liela ir nātrija hidroksīda masa šķīdumā?
Cik liels ir nātrija hidroksīda daudzums šķīdumā?
Cik liels 0,2 M sērskābes šķīduma tilpums ir nepieciešams, lai pilnībā neitralizētu šķīdumu, kas satur 0,25 mol nātrija hidroksīda?
4. uzdevums. (10 punkti)
Vielas sastāvā ir ogleklis (masas daļa savienojumā ir 24,24%), ūdeņradis (4,04%) un hlors. Vielas tvaiku blīvums pret gaisu ir 3,414.
Nosakiet vielas molekulārformulu!
Sastādiet vielas divu izomēru struktūrformulas un uzrakstiet to nosaukumus!
5. uzdevums. (11 punkti)
Attēlā ir redzama laboratorijas iekārta sērudeņraža sadedzināšanai skābeklī. Lai realizētu šo procesu, izmanto skābekli, sālsskābi un dzelzs(II) sulfīdu.

Nosauciet iekārtas galvenās sastāvdaļas!
Uzrakstiet, norādīto vielu formulas!
Uzrakstiet reakciju vienādojumus, kas norisinās aparātā 1 un traukā 3!
Kādā tilpumu attiecībā ir jāsajauc sērūdeņradis un skābeklis, lai vielas pilnībā izreaģētu?
Cik liels tilpums gaisa nepieciešams pilnīgai 0,4 l (n. a.) sērūdeņraža sadedzināšanai?
6. uzdevums. (12 punkti)
Rūpniecībā etanolu var iegūt dažādi. Vēsturisks paņēmiens ir ogļhidrātu hidrolīze un raudzēšana. Izmanto arī metodi, pēc kuras etilspirtu sintezē no etilēna.
Uzrakstiet cietes un saharozes hidrolīzes reakciju vienādojumus!
Uzrakstiet glikozes alkoholiskās rūgšanas reakcijas vienādojumu!
Uzrakstiet reakcijas vienādojumu, kas attēlo etanola sintētiskās iegūšanas metodi!
Miniet vienu Latvijas ražotni, kura ražo (vai arī ražoja) etanolu!
Redzama laboratorijas iekārta, kuru izmanto etanola izdalīšanai no maisījumiem.
Kādu fizikālu attīrīšanas paņēmienu izmanto šajā iekārtā?
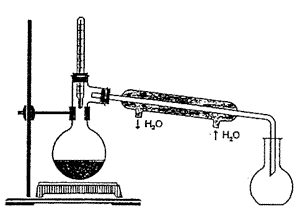
Rūpnieciski iegūtais etanols satur apmēram 4,5% ūdens. Šajā procesā ūdeni no etanola atdalīt nav iespējams, tāpēc tam pievieno ūdensatņēmējas vielas, piemēram, kalcija oksīdu. Aprēķiniet, cik liela masa kalcija oksīda jāpievieno 1 litram etanola (blīvums 0,8 g/cm3), kas satur 4,5% ūdens, lai iegūtu bezūdens etanolu!
Kāpēc ūdeni nav iespējams pilnīgi atdalīt no spirta, izmantojot fizikālo attīrīšanas paņēmienu?
7. uzdevums. (9 punkti)
Fosforu iegūst no dabiskajiem fosfātiem, tos reducējot elektriskā loka krāsnīs ar ogles un kvarca smilšu maisījumu.
Sastādiet fosfora iegūšanas molekulāro un oksidēšanās-reducēšanās reakcijas vienādojumu!

Zīmējumā A ir attēlota______fosfora, bet zīmējumā B -______fosfora uzbūve.
Miniet piemēru katra fosfora alotropiskā veida praktiskam pielietojumam!
Elements fosfors ietilpst dažādu fosforskābju un to sāļu sastāvā. Kāpēc mazgāšanas līdzekļiem pievieno dažādus fosfātus?
Kādu vielu izmanto ortofosfātjonu pierādīšanai? Sastādiet molekulāro un jonu vienādojumus! Ko novēro reakcijas rezultātā?
Kādas izmaiņas apkārtējā vidē var notikt, ja upēs un ezeros nonāk notekūdeņi, kas satur fosfātus?